程颖教授:帕博利珠单抗联合化疗为晚期肺鳞癌带来长期生存,助力肺癌慢病化进程
肺癌是常见的恶性肿瘤,肺鳞癌是其独特的组织学亚型,约占肺癌的25%左右。肺鳞癌预后更差且进展缓慢,标准化疗未满足转移性肺鳞癌患者治疗需求,且绝大多数患者无靶向治疗机会。基于KEYNOTE-407研究,帕博利珠单抗联合化疗成为晚期肺鳞癌领域首个获批的免疫联合化疗方案。近期KEYNOTE-407研究3年随访数据重磅公布,【肿瘤资讯】特别采访到吉林省肿瘤医院程颖教授,对于研究数据进行解读,畅谈免疫治疗的长生存。

程颖,二级教授,博士研究生导师,博士后工作站导师,享受国务院特殊津贴,卫生部突出贡献中青年专家,吉林省肿瘤医院党委书记,吉林省癌症中心主任,吉林省肿瘤医院恶性肿瘤临床研究一体化诊疗中心主任,吉林省肺癌诊疗中心主任。中国临床肿瘤学会(CSCO) 副理事长;CSCO小细胞肺癌专业委员会主任委员;CSCO临床研究专家委员会候任主任委员;中国抗癌协会肺癌专业委员会副主任委员;CSCO非小细胞肺癌专业委员会副主任委员;CSCO肿瘤大数据专家委员会副主任委员;中华医学会肿瘤学分会肺癌专委会副主任委员;中国医师协会肿瘤多学科诊疗专委会副主任委员;中国医师协会肺癌培训专业委员会副主任委员;全国医师定期考核肿瘤专业编辑专业委员会副主任委员;国家卫生、计生委常见肿瘤规范化诊疗专家组成员;吉林省医师协会肿瘤医师分会主任委员;吉林省医学会肿瘤专业委员会主任委员;担任《中华肿瘤杂志》等多家杂志编委。
在2021年欧洲肺癌大会上,KEYNOTE-407研究的3年随访数据重磅公布,能否请您介绍下最新的研究结果,谈谈最新数据对临床实践的意义?
程颖教授:KEYNOTE-407研究是一项全球多中心、随机、双盲、安慰剂对照的Ⅲ期临床研究,比较帕博利珠单抗或安慰剂联合白蛋白紫杉醇/紫杉醇+卡铂方案一线治疗转移性鳞状NSCLC的有效性和安全性,主要研究终点是总生存期(OS)和无进展生存期(PFS),次要研究终点包括客观缓解率(ORR)、缓解持续时间(DOR)和安全性,探索性终点为PFS2(定义为从随机开始至第二次疾病进展或死亡的时间)。
在2018年美国临床肿瘤学会(ASCO)年会上,首次报道了期中分析时的PFS和OS数据,研究共入组559例患者,帕博利珠单抗联合化疗组和安慰剂联合化疗组分别入组278和281例患者,中位随访时间为7.8个月时,两组OS的成熟度分别为30.6%和42.7%,PFS成熟度分别为54.7%和70.1%,结果显示,帕博利珠单抗联合化疗和安慰剂联合化疗组的中位OS分别为15.8个月和11.3个月(HR=0.64,P<0.001),两组的中位PFS分别为6.4个月和4.8个月(HR=0.56,P<0.001),与安慰剂联合化疗相比,帕博利珠单抗联合化疗显著改善了患者的PFS和OS,两组≥3级不良事件(AE)的发生率分别为69.8%和68.2%,免疫联合化疗安全性可控。该结果于2018年9月发表在《新英格兰医学杂志》(The New England Journal of Medicine,NEJM),2018年10月美国FDA批准帕博利珠单抗联合化疗一线治疗晚期肺鳞癌的适应证,这也是肺鳞癌领域首个免疫联合化疗的方案获批。
在2019年欧洲肿瘤内科学会(ESMO)年会上报道了最终分析结果,中位随访时间为14.3个月,帕博利珠单抗联合化疗组和安慰剂联合化疗组OS成熟度分别为60.4%和70.1%,PFS成熟度分别为78.1%和89.7%,结果显示,两组的中位OS分别为17.1个月和11.6个月(HR=0.71,95%CI 0.58~0.88),两组的中位PFS分别为8.0个月和5.1个月(HR=0.57,95%CI 0.47~0.69),PFS和OS持续获益,两组≥3级AE的发生率分别为74.1%和69.6%。该研究也首次报道了PFS2结果,两组的中位PFS2分别为13.9个月和9.1个月(HR=0.59,95%CI 0.49~0.72),说明即使研究允许化疗组进展后交叉给予帕博利珠单抗治疗,一线帕博利珠单抗联合化疗仍具有更长的PFS2,研究结果支持一线使用免疫治疗,研究结果于2020年6月发表在《胸部肿瘤学杂志》(Journal of Thoracic Oncology,JTO)。
在今年3月份举行的欧洲肺癌大会上,KEYNOTE-407研究公布了3年随访数据,中位随访时间为40.1个月,帕博利珠单抗联合化疗组和安慰剂联合化疗组OS成熟度分别为73.4%和81.9%,PFS成熟度分别为83.1%和91.5%。结果显示,帕博利珠单抗联合化疗的患者PFS和OS仍持续获益,与安慰剂联合化疗相比,免疫联合化疗组疾病死亡风险降低29%(中位OS:17.2 vs 11.6个月;HR=0.71),使疾病进展风险下降达41%(中位PFS:8.0 vs 5.1个月;HR=0.59),PFS和OS与之前报道的数据相仿;两组3年OS率分别为29.7%和18.2%,其中在PD-L1≥1%人群,两组3年OS率分别为33.4%和19.3%,在PD-L1<1%人群,两组3年OS率分别为22.1%和16.4%,在PD-L1表达阳性人群,免疫联合化疗具有更高的3年OS率。两组3年PFS率分别为16.1%和6.5%。接近20%(55/278)的患者完成了35个周期帕博利珠单抗治疗,此部分患者的ORR高达92.7%,中位DOR仍未达到;经过长期的随访,两组≥3级AE的发生率分别为74.8%和70.0%,延长随访时间并没有增加联合治疗组3级以上AE的发生率,患者总体耐受性良好。
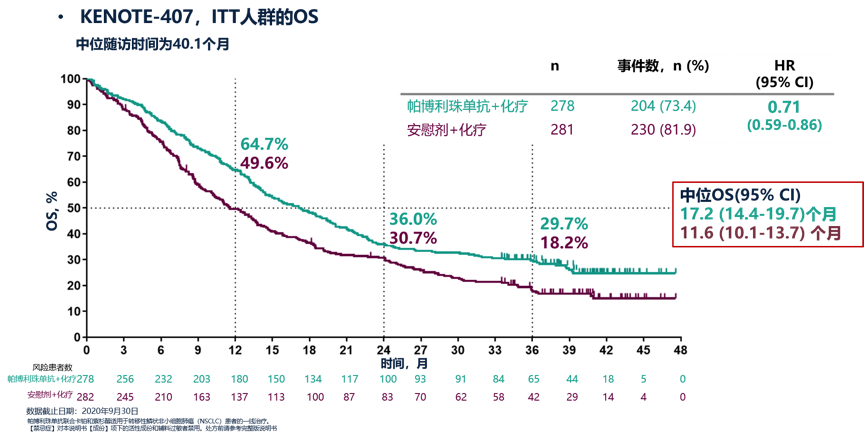
KEYNOTE-407研究3年随访OS数据[1]
KEYNOTE-407研究是首个报道晚期肺鳞癌一线免疫联合化疗3年OS数据的Ⅲ期临床研究,结果提示无论PD-L1的表达状态如何,免疫联合化疗均具有长期生存获益优势,且治疗后得到客观缓解的患者,更可能获得长期生存的机会,延长随访时间,免疫联合化疗也未出现足球app排行榜的毒副反应。该研究结果进一步巩固了帕博利珠单抗联合化疗作为晚期肺鳞癌患者标准一线治疗的地位,帕博利珠单抗联合紫杉醇/白蛋白紫杉醇+卡铂是优选的一线治疗方案。
2019年11月,国家药品监督管理局(NMPA)批准了帕博利珠单抗联合卡铂和紫杉醇适用于转移性鳞状NSCLC的一线治疗适应证,在中国人群中,该方案的疗效如何?
程颖教授:在KEYNOTE-407研究全球队列中,仅纳入了少量的中国患者(n=10),为了在中国获批适应证,在中国人群中进行了扩展队列研究。在2019年11月23日举行的ESMO Asia会议上,我代表中国13家研究中心报道了中国人群的数据,共入组125例患者,其中包括全球队列中10例患者和中国扩展队列115例患者。结果显示,免疫联合化疗组和安慰剂联合化疗组的中位OS分别为17.3个月和12.6个月(HR=0.44,95%CI 0.24~0.81),两组的中位PFS分别为8.3和4.2个月(HR=0.32,95%CI 0.21~0.49)。中国人群与全球人群数据对比,OS和PFS结果整体上与全球数据基本保持一致,在降低疾病的死亡风险方面,中国扩展队列研究和全球队列研究OS的HR值分别为0.44和0.71,帕博利珠单抗联合化疗在中国人群有更好的总生存获益趋势。基于这样的研究结果,在KEYNOTE-407中国扩展研究结果公布2天后,NMPA就批准了帕博利珠单抗联合卡铂和紫杉醇一线治疗转移性鳞状NSCLC的适应证,填补了近二十年来中国晚期肺鳞癌治疗史的空白,开启中国肺鳞癌免疫一线治疗新时代。此次,KEYNOTE-407全球人群长期随访结果公布,我们也有信心免疫治疗在中国人群中同样可以获得长期生存,改善中国晚期肺鳞癌患者的生存现状。
目前在驱动基因阴性晚期NSCLC的一线治疗上,您如何看待K药为患者所带来的长期生存?
程颖教授:目前,免疫治疗已经成为驱动基因阴性的晚期NSCLC患者极其重要的治疗手段,帕博利珠单抗单药治疗或联合化疗一线治疗均显示了良好的疗效,近期多项临床研究公布了长期的生存数据。KEYNOTE-024是一线免疫治疗首个公布5年生存数据的Ⅲ期临床研究,在PD-L1高表达(TPS≥50%)人群中,帕博利珠单抗单药治疗和化疗两组5年OS率分别为31.9%和16.3%,近三分之一的PD-L1高表达患者接受免疫单药治疗生存5年以上。
KEYNOTE-042研究也报道了3年生存数据,在PD-L1≥1%的晚期NSCLC患者中,帕博利珠单抗单药和化疗两组的3年OS率分别为25%和17%,其中在PD-L1≥50%人群中,两组3年OS率分别为31%和18%。KEYNOTE-189首次报道了非鳞NSCLC患者免疫联合化疗3年OS数据,帕博利珠单抗联合培美曲塞/铂类治疗和单独化疗的3年OS率分别为31.3%和17.4%,在PD-L1≥50%、1~49%和<1%人群中免疫联合化疗3年的OS率分别为43.7%、28.3%和23.3%。
此次KEYNOTE-407是首个报道鳞癌患者免疫联合化疗3年OS数据的Ⅲ期研究,帕博利珠单抗联合紫杉醇/白蛋白紫杉醇+卡铂的3年OS率29.7%,而单独化疗组为18.2%,在PD-L1≥1%和<1%人群中免疫联合化疗3年的OS率分别为33.4%和22.1%。多项临床研究结果显示,帕博利珠单抗一线治疗无论是单药使用还是联合化疗,患者均能够获得长期的生存获益;无论PD-L1的表达状态如何,帕博利珠单抗联合化疗均具有长期生存优势,但PD-L1表达阳性人群生存获益更大;而且,这种长期生存获益与组织学病理类型无关,无论是鳞癌或非鳞癌患者,长期生存数据基本一致,这些研究结果也说明了帕博利珠单抗一线治疗可以获得稳健的长期生存结果。
帕博利珠单抗作为PD-1/PD-L1抑制剂的代表,反映了免疫治疗后缓解持续时间长、患者获得长期生存的共性特点,这种长期生存获益由免疫治疗的独特机制所决定的。免疫治疗通过解除免疫抑制,可以激活T细胞,重新启动抗肿瘤免疫应答反应,能够持续识别和记忆肿瘤抗原,且随着时间不断增强和扩大,抗肿瘤免疫循环不断重复,抗肿瘤免疫反应持续加强;同时,免疫记忆功能随着免疫应答的扩大,一些细胞毒性T细胞分化为成熟记忆T细胞,即使在原始抗原刺激不存在时,这些细胞依然能够提供长期免疫记忆保护。这种效应也体现在免疫治疗的生存曲线中,生存曲线存在显著的“长拖尾效应”,即随着随访时间的延长生存曲线而愈发趋于平缓。因此,免疫治疗可以让晚期的肿瘤患者得到长期生存,让肺癌逐渐成为了一种可控的慢性疾病。











 吉公网安备 22017302000289号
吉公网安备 22017302000289号